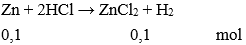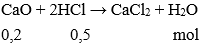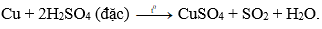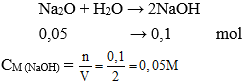Lý thuyết Hóa học 9 Chương 1 (mới 2022 + 25 câu trắc nghiệm): Các loại hợp chất vô cơ
Với tóm tắt lý thuyết Hóa học lớp 9 Các loại hợp chất vô cơ hay, chi tiết cùng với 25 câu hỏi trắc nghiệm chọn lọc có đáp án giúp học sinh nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn Hóa học lớp 9.
Hóa học 9 Chương 1: Các loại hợp chất vô cơ
A. Lý thuyết Các loại hợp chất vô cơ
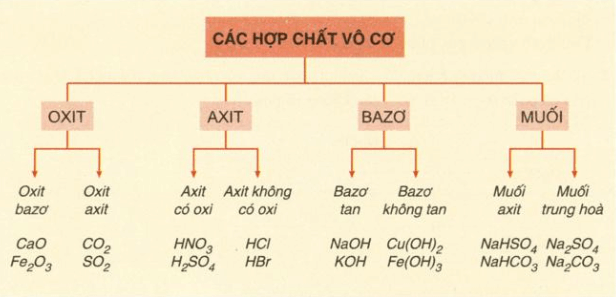
Bảng 1: Hệ thống, phân loại các hợp chất vô cơ:
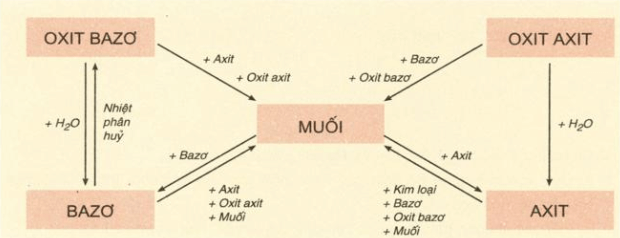
Bảng 2: Tính chất hóa học cơ bản của các hợp chất vô cơ
B. Trắc nghiệm Các loại hợp chất vô cơ
Câu 1: Có 3 lọ mất nhãn đựng riêng biệt 3 dung dịch của 3 chất: HCl, Na2SO4, NaOH . Chỉ dùng một hóa chất nào sau đây để phân biệt chúng ?
A. Dung dịch BaCl2
B. Quỳ tím
C. Dung dịch Ba(OH)2
D. Zn
Đáp án: B
Sử dụng quỳ tím:
+ Quỳ tím chuyển sang màu đỏ → HCl
+ Quỳ tím chuyển sang màu xanh → NaOH
+ Quỳ tím không chuyển màu → Na2SO4.
Câu 2: Khi cho từ từ dung dịch NaOH cho đến dư vào ống nghiệm đựng dung dịch hỗn hợp gồm HCl và một ít phenolphtalein. Hiện tượng quan sát được trong ống nghiệm là:
A. Màu đỏ mất dần.
B. Không có sự thay đổi màu
C. Màu đỏ từ từ xuất hiện.
D. Màu xanh từ từ xuất hiện.
Đáp án: C
Trong dung dịch sau phản ứng có NaOH dư làm cho phenolphtalein chuyển sang màu đỏ.
Câu 3: Cho 0,1mol kim loại kẽm vào dung dịch HCl dư. Khối lượng muối thu được là:
A. 13,6 g
B. 1,36 g
C. 20,4 g
D. 27,2 g
Đáp án: A
→ mmuối = 0,1.(65 + 35,5.2) = 13,6 gam.
Câu 4: Cho 0,2 mol Canxi oxit tác dụng với 500ml dung dịch HCl 1M. Khối lượng muối thu được là:
A. 2,22 g
B. 22,2 g
C. 23,2 g
D. 22,3 g
Đáp án: B
nHCl = 0,5.1 = 0,5 mol
Có 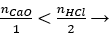
mmuối = 0,2. (40 + 71) = 22,2 gam.
Câu 5: Dung dịch axit clohiđric tác dụng với sắt tạo thành:
A. Sắt (II) clorua và khí hiđrô.
B. Sắt (III) clorua và khí hiđrô.
C. Sắt (II) Sunfua và khí hiđrô.
D. Sắt (II) clorua và nước.
Đáp án: A
Fe + 2HCl → FeCl2 + H2
Câu 6: Dung dịch muối tác dụng với dung dịch axit clohiđric là:
A. Zn(NO3)2
B. NaNO3.
C. AgNO3.
D. Cu(NO3)2.
Đáp án: C
AgNO3 + HCl → AgCl ↓ + HNO3
Câu 7: Axit sunfuric đặc nóng tác dụng với đồng kim loại sinh ra khí:
A. CO2.
B. SO2.
C. SO3.
D. H2S.
Đáp án: B
Câu 8: Dãy các kim loại đều tác dụng với dung dịch axit clohiđric:
A. Al, Cu, Zn, Fe.
B. Al, Fe, Mg, Ag.
C. Al, Fe, Mg, Cu.
D. Al, Fe, Mg, Zn.
Đáp án: D
Cu và Ag không tác dụng với axit HCl.
Câu 9: Thuốc thử để nhận biết dung dịch Ca(OH)2 là
A. K2CO3
B. KCl
C. KOH
D. KNO3
Đáp án: A.
Ca(OH)2 + K2CO3 → CaCO3 ↓ + 2KOH
Câu 10: Hòa tan 3,1 gam Na2O vào nước được 2 lít dung dịch. Nồng độ mol của dung dịch thu được là:
A. 0,05 M
B. 0,1 M
C. 0,3M
D. 0,4M
Đáp án: A
Số mol Na2O = 3,1 : 62 = 0,05 mol
Câu 11: Nhóm chất tác dụng với dung dịch HCl và với dung dịch H2SO4 loãng là:
A. CuO, BaCl2, ZnO
B. CuO, Zn, ZnO
C. CuO, BaCl2, Zn
D. BaCl2, Zn, ZnO
Đáp án: B
Câu 12: Để làm sạch dung dịch FeCl2 có lẫn tạp chất CuCl2 ta dùng:
A. H2SO4 .
B. HCl.
C . Al.
D. Fe.
Đáp án: D
Câu 13: Nhôm hoạt động hoá học mạnh hơn sắt, vì:
A. Al, Fe đều không phản ứng với HNO3 đặc nguội.
B. Al có phản ứng với dung dịch kiềm.
C. Nhôm đẩy được sắt ra khỏi dung dịch muối sắt.
D. Chỉ có sắt bị nam châm hút.
Đáp án: C
Câu 14: Dãy các bazơ bị phân hủy ở nhiệt độ cao:
A.Ca(OH)2, NaOH, Zn(OH)2, Fe(OH)3
B. Cu(OH)2, NaOH, Ca(OH)2, Mg(OH)2
C.Cu(OH)2, Mg(OH)2, Fe(OH)3, Zn(OH)2
D. Zn(OH)2, Ca(OH)2, KOH, NaOH
Đáp án: C
Câu 15: Dẫn 22,4 lít khí CO2 ( đktc) vào 200g dung dịch NaOH 20%. Sau phản ứng tạo ra sản phẩm nào trong số các sản phẩm sau:
A. Muối natricacbonat và nước.
B. Muối natri hidrocacbonat
C. Muối natricacbonat.
D.Muối natrihiđrocacbonat và natricacbonat
Đáp án: B
Câu 16: Hòa tan 12,2 gam hỗn hợp MgO và Al2O3 vào dung dịch HCl 20% thu được 31,45 gam hỗn hợp muối. Mặt khác, để trung hòa lượng axit dư cần dùng 20ml dung dịch NaOH 2M. Khối lượng dung dịch HCl ban đầu là:
A. 27,01 gam
B. 108,04 gam
C. 135,05 gam
D. 54,02 gam
Đáp án: C
Câu 17: Đốt cháy hoàn toàn một kim loại A có khối lượng 4,05 gam trong bình chứa oxi dư, sau phản ứng thu được 7,56 gam oxit của kim loại A. Hòa tan hoàn toàn lượng oxit trên bằng dung dịch HCl 20%, khối lượng dung dịch axit HCl đã dùng là:
A. 41,06 gam
B. 54 gam
C. 10,15 gam
D. 80,3 gam
Đáp án: D
Câu 18: Dùng hết 5kg than (chứa 90% C và 10% tạp chất không cháy) để đun nấu. Thể tích không khí cần dùng là bao nhiêu?
A. 40 m3
B. 41 m3
C. 42 m3
D. 45 m3
Đáp án: C
Câu 19: Cho phản ứng quang hợp của cây xanh:
6CO2 + 6H2O → C6H12O6 + 6CO2
Biết rắng mỗi hecta cây trồng mỗi ngày hấp thụ khoảng 374 kg CO2 thì thải vào không khí khối lượng oxi bằng bao nhiêu?
A. 272 kg
B. 220 kg
C. 252 kg
D. 300 kg
Đáp án: A
Câu 20: Cho 307 gam Na2CO3 tsc dụng với 365 gam dung dịch HCl nồng độ a%. Sau phản ứng thu được dung dịch muối có nồng độ 9%. a có giá trị là:
A. 10
B. 15
C. 5
D. 20
Đáp án: A
Câu 21: Hòa tan hoàn toàn 10,2 gam một oxit kim loại có hóa trị III cần vừa đủ 331,8 gam dung dịch H2SO4. Dung dịch muối sau phản ứng có nồng độ 10%. Công thức phân tử của oxit trên là:
A. Fe2O3
B. Al2O3
C. Cr2O3
D. Mn2O3
Đáp án: B
Câu 22: Cho Ba(OH)2 dư vào dung dịch chứa FeCl3, CuSO4, AlCl3 thu được kết tủa. Nung kết tủa đến thu được trong không khí đến khi có khối lượng không đổi thu được chất rắn X. Trong chất rắn X gồm:
A. FeO, CuO, Al2O3
B. Fe2O3, CuO, BaSO4
C. Fe3O4, CuO, BaSO4
D. Fe2O3, CuO
Đáp án: B
Câu 23: Thuốc thử để phân biệt dung dịch natrisunfat và dung dịch natri cacbonat là:
A. Axit clohidric
B. Chì (II) nitrat
C. Bạc nitrat
D. Bari clorua
Đáp án: A
Câu 24: Thêm từ từ dung dịch H2SO4 10% vào một dung dịch muối cacbonat của kim loại hóa trị I cho tới khi khí CO2 vừa thoát ra hết thì thu được dung dịch muối sunfat có nồng độ 13,63%. Công thức phân tử của muối cacbonat trên là:
A. K2CO3
B. Na2CO3
C. LiCO3
D. Li2CO3
Đáp án: B
Câu 25: Tìm công thức phân tử của hợp chất chứa 40% Cu, 20% S và 40% O, biết rằng trong phân tử chỉ có 1 nguyên tử lưu huỳnh.
A. CuSO3
B. CuSO4
C. CuSO2
D. Cu2SO4
Đáp án: C