Bài tập luyện tập về rượu Etylic, axit Axetic và chất Béo – Hóa 9 bài 48
Rượu Etylic C 2 H 5 OH axit Axetic CH 3 COOH và chất béo (có nhiều trong mỡ động vật và dầu thực vật) là nội dung kiến thức mà các em đã được học ở các bài trước.
Trong bài này chúng ta cùng tính chất của Rượu Etylic (ancol etylic hoặc etanol), axit Axetic và chất béo và đặc biệt là vận dụng các tính chất này trong việc giải một số bài tập về rượu etylic, axit Axetic và chất béo.
A. Tóm tắt lý thuyết về rượu Etylic, axit Axetic và chất béo
I. Rượu Etylic
1. Công thức cấu tạo của rượu Etylic
– Công thức cấu tạo: CH3-CH2-OH
2. Tính chất vật lý của rượu Etylic
– Rượu etylic (ancol etylic hoặc etanol) C2H5OH là chất lỏng, không màu, sôi ở 78,3oC, nhẹ hơn nước, tan vô hạn trong nước và hòa tan được nhiều chất như iot, benzen,…
3. Tính chất hóa học của rượu Etylic
• Phản ứng cháy của rượu Etylic
C2H5OH + 3O2 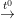 2CO2 + 3H2O
2CO2 + 3H2O
• Etylic tác dụng với Na
2C2H5OH + Na → 2C2H5ONa + H2
• Etylic tác dụng với axit axetic
CH3COOH + HO–C2H5 ←H2SO4(đặc,nóng)→ CH3COOC2H5 + H2O.
axit axetic etylic etylaxetat
II. Axit Axetic
1. Công thức cấu tạo axit Axetic
– Công thức cấu tạo rút gọn: CH3-COOH
2. Tính chất vật lý của axit Axetic
– Axit axetic CH3COOH là chất lỏng, không màu, vị chua, tan vô hạn trong nước.
3. Tính chất hóa học của axit axetic
• Axit axetic cũng có đầy đủ tính chất của một axit, nhưng là một axit yếu.
– Dung dịch axit axetic làm quỳ tím đổi thành màu đỏ.
– Axit axetic tác dụng với oxit bazơ, bazơ tạo thành muối và nước.
CH3COOH + NaOH → H2O + CH3COONa (Natri axetat)
2CH3COOH + Na2CO3 → 2CH3COONa + CO2 + H2O
– Axit Axetic tác dụng với ancol etylic tạo ra este và nước
CH3COOH + HO-C2H5 ←H2SO4(đặc,nóng)→ CH3COO C2H5 + H2O
III. Chất Béo
1. Công thức cấu tạo của chất béo
• Chất béo là hỗn hợp nhiều este của glixerol với các axit béo và có công thức chung là (R-COO)3C3H5.
– Trong đó R có thể là C17H35- ; C17H33- ; C15H31-;…
2. Tính chất vật lý của chất béo
– Chất béo có nhiều trong dầu, mỡ. Mỡ ở thể rắn, còn dầu ở thể lỏng.
– Chất béo nhẹ hơn nước, không tan trong nước, tan được trong dầu hỏa, xăng,…
3. Tính chất hóa học của chất béo
• Thủy phân trong môi trường axit :
(RCOO)3C3H5 + 3H2O ![small xrightarrow[]{t^{0},axit}](https://hayhochoi.vn/uploads/news/wyswyg/2020_05/1588821040bl81lw0k5i.gif) 3RCOOH + C3H5(OH)3
3RCOOH + C3H5(OH)3
• Thủy phân trong môi trường kiềm:
(RCOO)3C3H5 + 3NaOH ![small xrightarrow[]{t^{0}}](https://hayhochoi.vn/uploads/news/wyswyg/2020_05/1588821042ixzlopgp32.gif) 3RCOONa + C3H5(OH)3
3RCOONa + C3H5(OH)3
B. Bài tập luyện tập về Rượu Etylic, Axit Axetic và chất béo
* Bài 1 trang 148 SGK Hóa học 9: Cho các chất sau: rượu etylic, axit axetic, chất béo. Hỏi:
a) Phân tử chất nào có nhóm – OH? Nhóm – COOH?
b) Chất nào tác dụng với K? với Zn? Với NaOH? Với K2CO3?
Viết các phương trình hóa học
° Lời giải bài 1 trang 148 SGK Hóa học 9:
a) Chất có nhóm – OH: rượu etylic (C2H5OH), CH3COOH.
Chất có nhóm – COOH: axit axetic (CH3COOH).
b) – Chất tác dụng được với K: rượu etylic và axit axetic:
2C2H5OH + 2K → 2C2H5OK + H2↑
2CH3COOH + 2K → 2CH3COOK + H2↑
– Chất tác dụng được với Zn: CH3COOH
2CH3COOH + Zn → (CH3COO)2Zn + H2↑
– Chất tác dụng được với NaOH : axit axetic và chất béo :
CH3COOH + NaOH → CH3COONa + H2O
(RCOO)3C3H5 + 3NaOH → C3H5(OH)3 + 3RCOONa
– Chất tác dụng với K2CO3: CH3COOH
2CH3COOH + K2CO3 → 2CH3COOK + CO2↑ + H2O.
* Bài 2 trang 148 SGK Hóa học 9: Tương tự chất béo, etyl axetat cũng có phản ứng thủy phân trong dung dịch axit và dung dịch kiềm. Hãy viết phương trình hóa học xảy ra khi đung etyl axetat với dung dịch HCl, dung dịch NaOH.
° Lời giải bài 2 trang 148 SGK Hóa học 9:
– Phản ứng của etyl axtat với dung dịch HCl:
CH3COOC2H5 + H2O ![small xrightarrow[]{t^{0},HCl}](https://hayhochoi.vn/uploads/news/wyswyg/2020_05/1588821044fmos7ugale.gif) CH3COOH + C2H5OH
CH3COOH + C2H5OH
– Phản ứng của etyl axtat với dung dịch NaOH.
CH3COOC2H5 + NaOH ![small small xrightarrow[]{t^{0}}](https://hayhochoi.vn/uploads/news/wyswyg/2020_05/1588821046j1h2aaryo4.gif) CH3COONa + C2H5OH
CH3COONa + C2H5OH
* Bài 3 trang 149 SGK Hóa học 9: Hãy chọn các chất thích hợp điền vào các dấu hỏi rồi hoàn thành các phương trình hóa học sau:
a) C2H5OH + ? → ? + H2
b) C2H5OH + ? → CO2 + ?
c) CH3COOH + ? → CH3COOK + ?
d) CH3COOH + ? → CH3COOC2H5 + ?
e) CH3COOH + ? → ? + CO2 + ?
g) CH3COOH + ? → ? + H2
h) Chất béo + ? → ? + muối của các axit béo.
° Lời giải bài 3 trang 149 SGK Hóa học 9:
a) 2C2H5OH + 2Na → 2C2H5ONa + H2
b) C2H5OH + 3O2 ![small small xrightarrow[]{t^{0}}](https://hayhochoi.vn/uploads/news/wyswyg/2020_05/1588821046j1h2aaryo4.gif) 2CO2 + 3H2O.
2CO2 + 3H2O.
c) 2CH3COOH + 2K → 2CH3COOK + H2.
d) CH3COOH + C2H5OH ←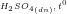 → CH3COOC2H5 + H2O
→ CH3COOC2H5 + H2O
e) 2CH3COOH + CaCO3 → (CH3COO)2Ca + CO2 + H2O.
g) 2CH3COOH + Mg → (CH3COO)2Mg + H2
h) Chất béo + Natri hidroxit → Glixerol + muối của các axit béo.
* Bài 4 trang 149 SGK Hóa học 9: Có ba lọ không nhãn đựng ba chất lỏng là: rượu etylic, axit axetic và dầu ăn tan trong rượu etylic. Chỉ dùng nước và quỳ tím, hãy phân biệt các chất lỏng trên.
° Lời giải bài 4 trang 149 SGK Hóa học 9:
– Trích mẫu thử và đánh số thứ tự.
– Lần lượt nhúng quỳ tím vào 3 mẫu thử trên
+ Mẫu làm quỳ tím hóa đỏ là axit axetic.
+ 2 mẫu còn lại không có hiện tượng gì.
– Cho hai chất lỏng còn lại cho vào nước, chất nào tan hoàn toàn đó là rượu etylic, còn lại là hỗn hợp dầu ăn (dầu ăn sẽ tan trong rượu etylic).
* Bài 5 trang 149 SGK Hóa học 9: Khi xác định công thức của các chất hữu cơ A và B, người ta thấy công thức phân tử của A là C2H6O, còn công thức phân tử của B là C2H4O2. Để chứng minh A là rượu etylic, B là axit axetic cần phải làm thêm những thí nghiệm nào? Viết phương trình hóa học minh họa (nếu có).
° Lời giải bài 5 trang 149 SGK Hóa học 9:
– Ta có PTHH:
2C2H5OH + 2Na → 2C2H5ONa + H2↑.
– Ứng với CTPT: C2H6O, ta sẽ có 2 công thức cấu tạo
CH3 – O – CH3 và CH3 – CH2 – OH.
⇒ Để chứng tỏ A là rượu Etylc: Cho A tác dụng bới Na nếu có khí bay ra.
– Ứng với CTPT: C2H4O2 ta có các CTCT sau:
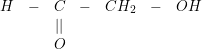
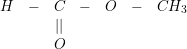
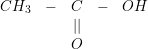
⇒ Để chứng tỏ B là axit axetic: Cho B tác dụng với Na2CO3 nếu có khí thoát ra.
2CH3COOH + Na2CO3 → 2CH3COONa + H2O + CO2↑
* Bài 6 trang 149 SGK Hóa học 9: Khi lên men dung dịch loãng của rượu etylic, người ta được giấm ăn.
a) Từ 10 lít rượu 8o có thể điều chế được bao nhiêu gam axit axetic? Biết hiệu xuất quá trình lên men là 92% và rượu etylic có D = 0,8 g/cm3.
b) Nếu pha khối lượng axit axetic trên thành dung dịch giấm 4% thì khối lượng dung dịch giấm thu được là bao nhiêu?
° Lời giải bài 6 trang 149 SGK Hóa học 9:
a) Trong 10 lít rượu 80 thì có: 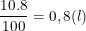 rượu etylic
rượu etylic
⇒ mrượu = V.D = 0,8.0,8.1000 = 640 (g)
⇒ 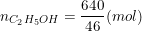
– Phương trình phản ứng lên men rượu:
C2H5OH + O2 → CH3COOH + H2O
– Theo PTPƯ thì: 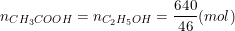
⇒ Khối lượng của axit: 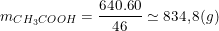
– Vì hiệu suất quá trình lên men là 92% nên lượng axit có trong thực tế thu được:
⇒ maxit = 834,8.92% = 768(g).
b) Khối lượng giấm thu được: 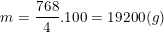
* Bài 7 trang 149 SGK Hóa học 9: Cho 100g dung dịch CH3COOH 12% tác dụng vừa đủ với dung dịch NaHCO3 8,4%.
a) Hãy tính khối lượng dung dịch NaHCO3 đã dùng.
b) Hãy tính nồng độ phần trăm của dung dịch muối thu được sau phản ứng.
° Lời giải bài 7 trang 149 SGK Hóa học 9:
– Ta có PTPƯ:
CH3COOH + NaHCO3 → CH3COONa + CO2↑ + H2O
1 (mol) 1 1 1
0,2 (mol) ? ? ?
a) Từ công thức C% = (mct/mdd).100% và theo bài cho 100g dung dịch CH3COOH 12% nên:
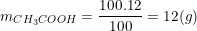
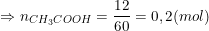
– Theo PTPƯ: nNaHCO3 = nCH3COOH = 0,2 (mol)
⇒ mNaHCO3 = 0,2. 84 = 16,8 (g)
⇒ Khối lượng dung dịch NaHCO3 là:
mdd (NaHCO3) = (mct/C%).100 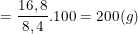
b) Theo PTPƯ: nCH3COONa = nCO2 = nCH3COOH = 0,2(mol)
⇒ mCH3COONa = 82. 0,2 = 16,4 (g)
⇒ mCO2 = 0,2. 44 = 8,8 (g)
⇒ Khối lượng dung dịch sau phản ứng là:
mdd = mCH3COOH + mNaHCO3 – mCO2 = 100 + 200 – 8,8 = 291,2 (g)
⇒ C%(CH3COONa) = (16,4/291,2).100 = 5,63 %






